商机详情 -
广东RNA免疫共沉淀RIP Seq检测
RIP-qPCR实验(RNA Immunoprecipitation followed by quantitative PCR)是一种用于研究细胞内特定蛋白质与RNA相互作用的技术。该技术结合了免疫沉淀(Immunoprecipitation)和实时荧光定量PCR(quantitative PCR,qPCR)的方法,旨在识别和定量与特定蛋白质结合的RNA分子。在RIP-qPCR实验中,首先使用针对目标蛋白质的特异性抗体进行免疫沉淀,将与该抗体结合的蛋白质-RNA复合物从细胞裂解液中分离出来。随后,通过洗涤步骤去除非特异性结合的分子,保留与目标蛋白质特异性结合的RNA。接下来,从免疫沉淀复合物中提取RNA,并将其逆转录为cDNA。然后,利用特异性引物进行qPCR反应,以定量检测与目标蛋白质结合的特定RNA分子的丰度。通过比较不同样品中目标RNA的相对表达水平,可以评估蛋白质与RNA之间的结合强度和特异性。RIP-qPCR实验在生物学研究中具有广泛应用,可用于研究转录后调控、RNA转运、RNA稳定性以及非编码RNA与蛋白质相互作用等方面的问题。该技术为揭示细胞内基因表达调控的复杂网络提供了有力工具。RIP-qpcr实验,有哪些优点。广东RNA免疫共沉淀RIP Seq检测
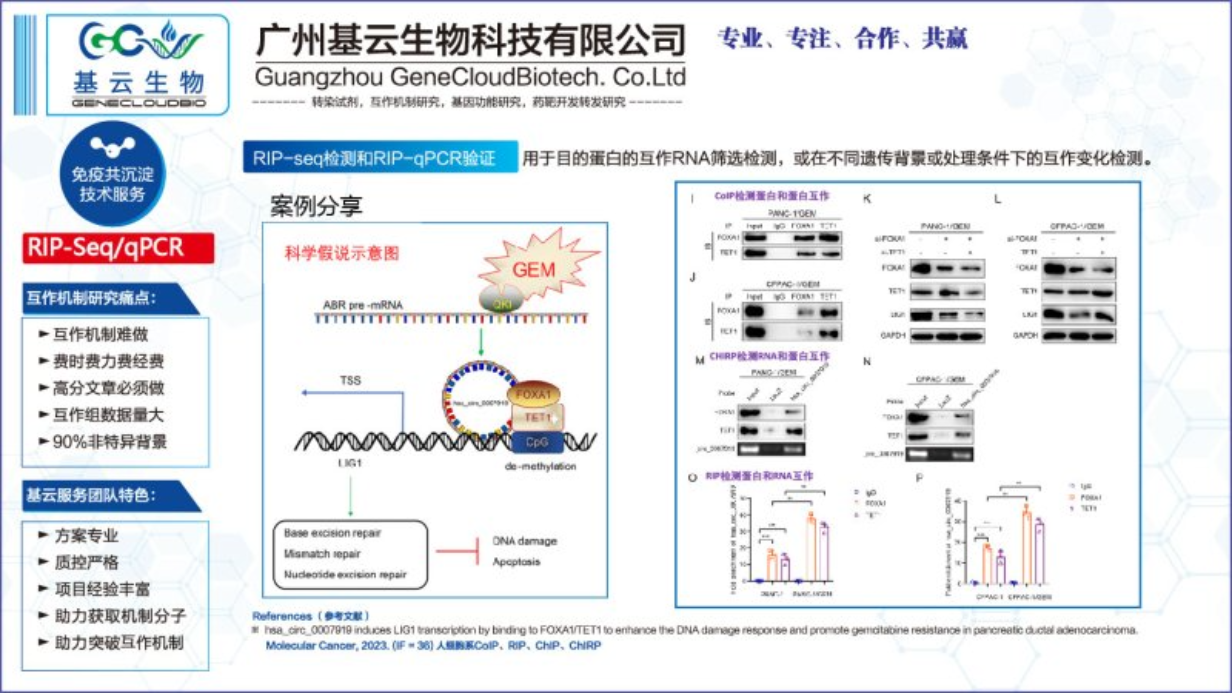
在分子机制研究过程中,RIP-qPCR实验技术扮演着重要角色。该技术主要应用于研究细胞内RNA与蛋白质的相互作用,有助于揭示基因表达的转录后调控机制。通过RIP-qPCR,研究者可以特异性地识别并结合目标RNA结合蛋白(RBP),进而分析与其结合的RNA分子。这一步骤对于理解RBP在细胞内的功能和调控网络至关重要。例如,在疾病研究中,RIP-qPCR可用于检测与疾病相关的RBP及其结合的RNA,从而揭示疾病发生和发展的分子机制。此外,RIP-qPCR还可用于验证生物信息学预测或高通量筛选结果,确认RNA与蛋白质之间的相互作用关系。这对于后续的功能研究和药物研发具有重要意义。总的来说,RIP-qPCR实验技术在分子机制研究中具有广泛的应用场景,特别是在研究RNA与蛋白质的相互作用、揭示转录后调控机制以及疾病相关分子机制等方面。然而,该技术也存在一些局限性,如抗体依赖性、RNA易降解等,因此在实际应用中需要谨慎选择和优化实验条件。尽管如此,随着技术的不断发展,RIP-qPCR仍将是分子机制研究领域的有力工具之一。广东RNA免疫共沉淀RIP Seq检测RIP-qPCR实验技术有哪些优缺点。
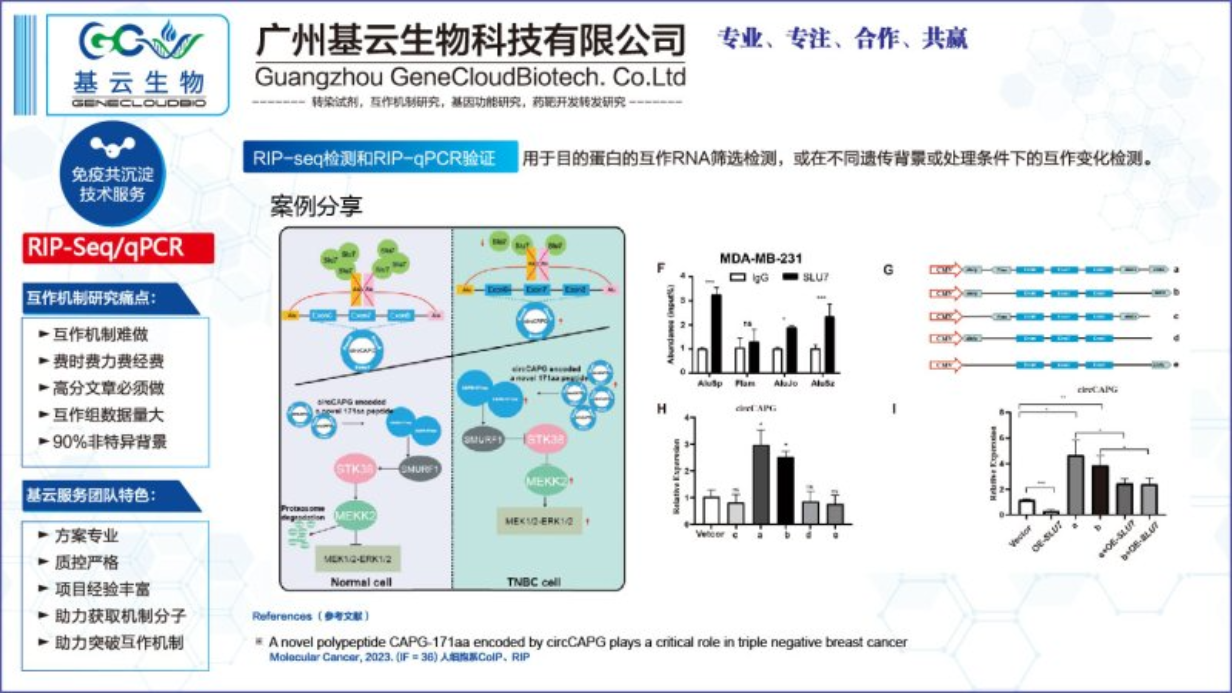
RIP实验RNA结合蛋白-RNA复合物的免疫沉淀(RIP)免疫沉淀方法:
将所有的试管在4°C下旋转孵育3小时至过夜。
将免疫沉淀管短暂离心,放置在磁性分离器上,弃用上清液。
从磁铁上取下试管。每管中加入0.5mLRIP洗涤缓冲液,短暂涡旋。(重复清洗5次)
在后面一次洗涤中,将500µL的珠子悬液中各取出50µL,通过免疫印迹法检测免疫沉淀的效率。在1XSDS-PAGE加载缓冲液中重新悬浮珠子,然后在95°C加热,可以洗脱蛋白质。然后可以离心,上清液直接应用于SDS-PAGE上。
进行RIP-qPCR实验,应该注意以下几个关键问题,以确保实验的成功和准确性。1. 样本处理:确保样本新鲜且未受污染,避免RNA降解。在处理过程中使用无RNase的试剂和耗材,并在冰上操作以维持低温环境。2. 抗体选择:选择特异性强的抗体进行免疫沉淀,这是实验成功的关键。验证抗体的特异性和效力,以确保准确捕捉目标RNA-蛋白质复合物。3. 引物设计:设计特异性针对目标RNA的引物,避免非特异性扩增。确保引物的质量和纯度,以获得可靠的qPCR结果。4. 实验对照:设置适当的对照实验,如使用非特异性抗体作为阴性对照,以验证实验结果的特异性和准确性。5. 操作规范:严格遵守RNA操作规范,避免RNA酶的污染。确保实验环境的清洁和无菌,以减少误差和干扰。6. 数据分析:使用适当的统计方法和软件分析实验数据,确保结果的准确性和可靠性。注意识别并排除异常值,以获得真实可信的结果。综上所述,进行RIP-qPCR实验时,你应注意样本处理、抗体选择、引物设计、实验对照、操作规范和数据分析等关键问题。通过仔细考虑和遵循这些注意事项,可以提高实验的成功率和准确性。进行RIP-qPCR实验时,引物设计时应注意哪些问题。

RIP-qPCR实验技术,是一种研究细胞内RNA与蛋白质相互作用的重要方法,具有广泛的应用场景。首先,在转录后调控研究中,RIP-qPCR可用于识别与特定RNA结合蛋白(RBP)相互作用的RNA分子,从而揭示RBP在转录后调控网络中的功能。这有助于深入了解基因表达的调控机制,包括mRNA稳定性、剪接和翻译等过程。其次,RIP-qPCR可用于验证生物信息学预测或高通量筛选结果。例如,在预测了某个RBP的潜在靶标RNA后,可以利用RIP-qPCR实验进行验证,确认它们之间的相互作用关系。此外,RIP-qPCR还可应用于疾病机制研究中。许多疾病的发生与发展与RNA与蛋白质的异常相互作用有关。通过RIP-qPCR技术,可以研究这些异常相互作用在疾病进程中的作用,为疾病的诊疗提供新的思路。另外,在药物研发领域,RIP-qPCR也具有潜在的应用价值。例如,可以研究药物对特定RNA-蛋白质相互作用的影响,从而评估药物的疗效和机制。总之,RIP-qPCR实验技术在转录后调控、生物信息学验证、疾病机制研究和药物研发等多个领域具有广泛的应用前景,为生物医学研究提供了有力的工具。RIP实验通常需要进行抗体预实验。抗体预实验在RIP实验中扮演着重要的角色。广东RNA免疫共沉淀RIP Seq检测
RIP和ChIP实验在研究对象、实验原理、实验操作、优化条件和技术应用等方面存在明显差异。广东RNA免疫共沉淀RIP Seq检测
RIP实验RNA纯化方法:
制备蛋白酶K缓冲液。每个免疫沉淀需要150µL蛋白酶K缓冲液,包含117µLRIP洗涤缓冲液,15µL10%SDS,18µL10mg/mL蛋白酶K。
在150µL的蛋白酶K缓冲液中悬浮每个免疫沉淀。
将第三节第4步的input样品解冻,在试管中加入107µLRIP洗涤缓冲液、15µL10%SDS和18µL蛋白酶K,使体积提高到150µL。
将所有试管在55°C下摇晃孵育30分钟以消化蛋白质。
孵育后,将管短暂离心,并将管放置在磁分离器上。将上清液转移到一个新的试管中。
在上清液的试管中加入250µLRIP洗涤缓冲液。
在每根试管中加入400µL的苯酚:氯仿:异戊醇。涡旋15秒,在室温下以14000rpm离心10分钟,以分离相位。
取出350μL水相,将其放入新管中。加入400µL的氯仿。涡旋15秒,在室温下以14000rpm离心10分钟,以分离相位。
取出300μL的水相,然后放入一个新的试管中。
在每根试管中加入50µL盐溶液I、15µL盐溶液II、5µL沉淀增强剂和850µL无水乙醇。混合并在-80°C下保持1小时至过夜,以沉淀RNA。
在4°C下以14000rpm离心30分钟,小心丢弃上清液。
用80%的乙醇清洗沉淀一次。在4°C下以14000rpm离心15分钟。小心地弃出上清液,晾干沉淀。重新悬浮在10到20µL的无RNase的水中,并将管子放在冰上。 广东RNA免疫共沉淀RIP Seq检测